Myasthenia gravis: Was steckt hinter der Muskelschwäche?
Myasthenia gravis bezeichnet eine chronische Autoimmunerkrankung, die mit einer Muskelschwäche einhergeht. Dabei leitet sich der Name Myasthenie von den griechischen Wörtern für Muskel (mys) und Krankheit (asthenia) ab. Gravis ist das lateinische Wort für schwer. Betroffen sind vor allem Menschen im vierten sowie im siebten bis achten Lebensjahrzehnt, wobei Frauen eher im jüngeren Alter betroffen sind und Männer eher mit steigendem Alter. Die Ursache der seltenen Erkrankung ist in vielen Fällen nicht festzustellen. Heutzutage ist durch eine erfolgreiche Therapie meist eine normale Lebenserwartung zu erreichen und die Prognose dementsprechend gut. Im Folgenden stellen wir Einzelheiten zu Symptomen, Diagnostik, Verlauf und Therapie der Erkrankung vor.
Was ist Myasthenia gravis?
Die Myasthenia gravis oder auch Myasthenia gravis pseudoparalytica ist eine neurologische Erkrankung. Sie wird durch Antikörper verursacht, die der menschliche Organismus selbst bildet. Damit gehört sie zur Gruppe der Autoimmunerkrankungen.
Vom Körper gebildete Antikörper richten sich normalerweise gegen körperfremde Substanzen, die potenziell schädlich für den Körper sind, zum Beispiel Bakterien oder Viren. Bei einer Fehlfunktion des Immunsystems kann es jedoch dazu kommen, dass Antikörper gegen körpereigene Strukturen (Autoantikörper) gebildet werden. Dies kann zu Entzündungsreaktionen mit entsprechenden Beschwerden führen.
Was passiert bei einer Myasthenia gravis im Körper?
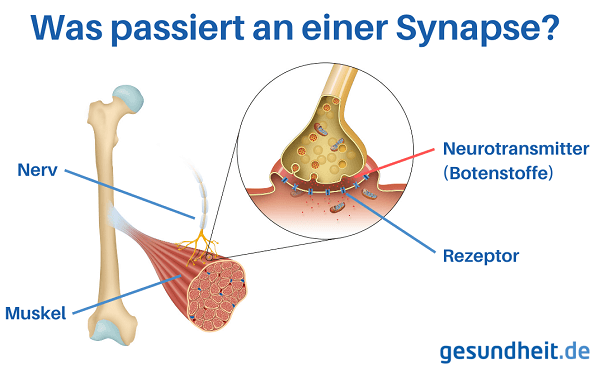
Bei der Myasthenia gravis werden Autoantikörper gegen den sogenannten Acetylcholin-Rezeptor an der Synapse (Kontaktstelle) zwischen Nervenzelle und Muskel gebildet. Der entsprechende Teil des Muskels wird auch motorische Endplatte genannt.
Als Rezeptoren bezeichnet man Teile einer Zelle, die für bestimmte Reize empfindlich sind, sozusagen Andockstellen für bestimmte Botenstoffe (Neurotransmitter). Acetylcholin-Rezeptoren sind Rezeptoren für den Botenstoff Acetylcholin. Sie kommen jedoch nicht nur an der motorischen Endplatte, sondern auch vielen anderen Stellen des menschlichen Körpers vor.
An der motorischen Endplatte wird Acetylcholin von den Nervenzellen ausgeschüttet und dockt im Normalfall an die Acetylcholin-Rezeptoren der Muskelzellen an. Im Anschluss kommt es zu einer Öffnung des Rezeptors, sodass Natrium- und Kaliumionen in die Muskelzelle einströmen können. Dies führt zu einer Erregung der Muskelzelle und ihrer Kontraktion. Vereinfacht gesagt: Die Nerven geben ein Signal, das über einen Botenstoff und einen Rezeptor zu den Muskeln gelangt – woraufhin diese sich anspannen.
Die Autoantikörper blockieren bei der Myasthenia gravis aber die Rezeptoren, sodass Acetylcholin nicht andocken kann und eine Erregung sowie die Kontraktion der Muskelzellen ausbleibt. Langfristig kommt es außerdem zu einer Zerstörung der Acetylcholin-Rezeptoren mit zunehmender Muskelschwäche.
Ursachen: Wie entsteht Myasthenia gravis?
Wie es zur Entstehung der Acetylcholin-Rezeptor-Antikörper kommt, was also die eigentliche Ursache der Krankheit ist, ist nicht vollständig geklärt.
Bei den meisten Betroffenen sind krankhafte Veränderungen des Thymus (Thymusdrüse) nachweisbar. Der Thymus ist Teil des lymphatischen Systems und am Aufbau des Immunsystems beteiligt. Während der Pubertät wird er nicht mehr benötigt und bildet sich zurück. Bei der Myasthenia gravis sind aber häufig Vergrößerung des Thymus (Thymushyperplasie) oder gar Neubildungen (Thymome) nachweisbar.
Außerdem besteht bei der Myasthenia gravis ein Zusammenhang mit anderen Autoimmunerkrankungen wie der Hashimoto-Thyreoiditis (Entzündung der Schilddrüse), der rheumatoiden Arthritis (Entzündung von Gelenken) und dem systemischen Lupus erythematodes (Entzündung verschiedenster Strukturen).
Symptome: Wie äußert sich eine Myasthenia gravis?
Das Hauptsymptom der Myasthenia gravis ist eine Muskelschwäche. Daraus ergeben sich weitere Symptome, die sich je nach betroffener Muskelgruppe unterscheiden. Folgende Formen werden unterschieden:
- okuläre Muskulatur: Herabhängen des Augenlids (Ptosis) auf einer oder beiden Seiten, Sehen von Doppelbildern (Diplopie), Lähmung von Augenmuskeln
- bulbäre Muskulatur: Schwierigkeiten beim Sprechen (Dysarthrie) und Schlucken (Dysphagie), schlaffe Gesichtszüge (Facies myopathica)
- Skelettmuskulatur: Schwäche der Extremitäten, Kopfhalteschwäche, in schweren Fällen: Schwäche der Atemmuskulatur mit Luftnot (Dyspnoe)
Die Symptome treten insbesondere bei wiederholter Belastung auf und nehmen im Tagesverlauf, bei Infekten, der Menstruation und Stresssituationen zu. Die Erkrankung kann also in Schüben verlaufen. Das Auftreten von Schmerzen ist möglich, in der Regel gehören Schmerzen jedoch nicht zu den Symptomen. Im Verlauf der Erkrankung kann es zur Abnahme von Muskelmasse (Muskelatrophie) kommen.
Wichtig zur Unterscheidung von anderen neurologischen Erkrankungen ist, dass keine Störungen der Berührungsempfindlichkeit (Sensibilität) und der Reflexe auftreten.
Ist Myasthenia gravis gefährlich?
Es handelt sich um eine ernstzunehmende, behandlungsbedürftige Erkrankung. Sie schränkt Betroffene in ihrem täglichen Leben stark ein und führt zu einer Reduktion der Lebensqualität. Um die Symptome zu lindern, ist häufig die lebenslange Einnahme von Medikamenten notwendig – jedoch ohne, dass die Erkrankung so geheilt werden kann. Durch die richtige Behandlung kann aber in vielen Fällen eine normale Lebenserwartung erreicht werden.
Gefahr geht vor allem von der krisenhaften Verschlechterung der Symptome im Rahmen einer sogenannten myasthenen Krise aus. Ursachen für eine solche Zunahme der Beschwerden können Medikamente sein, die Einfluss auf die neuromuskuläre Übertragung nehmen, aber auch Infektionen, Fieber sowie Narkosen bei Operationen. Im Vordergrund stehen bei der myasthenen Krise die Schwäche der Atemmuskulatur in Verbindung mit dem Unvermögen der Lunge, genügend Sauerstoff aufzunehmen (respiratorische Insuffizienz) und der Gefahr, dass Flüssigkeiten oder Feststoffe in die Lungen gelangen (Aspiration).
Zur Behandlung einer myasthenen Krise ist zwingend eine intensivmedizinische Therapie mit Sicherung der Atemwege und Verabreichung entsprechender Medikamente notwendig. Die Sterblichkeit dieses Krankheitsbildes liegt trotz intensivmedizinischer Therapie bei zwei bis drei Prozent.
Diagnostik einer Myasthenia gravis
Bei Verdacht auf eine Myasthenia gravis werden unterschiedliche Untersuchungen vorgenommen, um die Diagnose zu stellen.
Beurteilung der Muskelfunktion
Die Diagnostik beginnt mit der körperlichen Untersuchung des Patienten. Hierbei wird vor allem auf die Muskelkraft und eine Muskelermüdung bei wiederholter Beanspruchung geachtet. Es existieren mehrere Tests zur Beurteilung der Muskelfunktion:
- Simpson-Test: Durch Aufwärtsblick für eine Minute wird eine Ptosis, als das Herabhängen des Augenlids, provoziert.
- Halteversuch der Arme: Der Betroffene ist nicht dazu in der Lage, die Arme für 180 Sekunden gerade von sich wegzustrecken und in der Waagerechten zu halten.
- Halteversuch der Beine: Der Betroffene ist nicht dazu in der Lage, im Liegen die Beine für 45 Sekunden in einem 45°-Winkel zu halten.
- Halteversuch des Kopfes: Der Patient ist nicht dazu in der Lage, im Liegen den Kopf für 90 Sekunden in einem 45°-Winkel zu halten.
- Mimik-Test: Beurteilung des Lidschlusses je nach Stärke.
Edrophonium-Test
Des Weiteren existieren medikamentöse Tests, die die Auswirkung eines Cholinesterasehemmers auf die Symptomatik überprüfen (Edrophonium-Test, früher: Tensilon-Test). Dem Betroffenen wird dabei Edrophonium intravenös verabreicht. Es handelt sich dabei um einen Hemmer des Enzyms Cholinesterase. Die Cholinesterase ist dafür verantwortlich, den Botenstoff Acetylcholin abzubauen.
Wird dieses Enzym gehemmt, kommt es zu einer höheren Konzentration von Acetylcholin an der motorischen Endplatte und damit zu einer besseren Muskelfunktion. Dementsprechend sollte sich die Muskelschwäche unter Edrophonium innerhalb von 30 bis 60 Sekunden bessern.
Die Injektion von Cholinesterasehemmern ist mit einigen Risiken und Nebenwirkungen verbunden und sollte nur von einem erfahrenen Mediziner und unter Bereithaltung von Notfallausrüstung durchgeführt werden.
Labordiagnostik, elektrophysiologische Untersuchung und Bildgebung
Die letzte Säule der Diagnostik umfasst die Labordiagnostik, die elektrophysiologische Untersuchung der Muskulatur und die Bildgebung:
- Im Labor werden Antikörper gegen den Acetylcholin-Rezeptor nachgewiesen. Es können über fünf verschiedene Arten von Antikörpern nachgewiesen werden. Außerdem werden Routineparameter wie Blutbild, Schilddrüsenwerte und Entzündungswerte bestimmt.
- Die elektrophysiologische Untersuchung bezeichnet die Stimulation von Nerven mittels elektrischer Impulse. Diese Stimulationen haben normalerweise eine Muskelkontraktion, also eine Muskelanspannung, zur Folge, die gemessen wird. Die Muskelantwort nimmt bei der Myasthenia gravis von Stimulation zu Stimulation immer weiter ab. Dieses Phänomen wird als Dekrement bezeichnet. Eine Kombination mit dem Edrophonium-Test ist möglich. Hierbei sollte nach Gabe des Enzyms weniger oder kein Dekrement mehr nachweisbar sein.
- Die bildgebenden Verfahren Computertomographie (CT) und Magnetresonanztomographie (MRT) spielen vor allem zum Nachweis einer krankhaften Thymusveränderung eine Rolle.
Therapie: Welche Medikamente bei Myasthenia gravis?
Die Basis der Therapie einer Myasthenia gravis stellen die Cholinesterasehemmer dar, um die Muskelfunktion zu verbessern. Das Mittel der Wahl ist Pyridostigmin. Es kann in Tablettenform eingenommen werden. Die Einstellung, also die Festlegung der richtigen Dosis, sollte durch einen Spezialisten mit entsprechender Erfahrung erfolgen. Die Patienten müssen über die korrekte Einnahme sowie über mögliche Gefahren und Risiken aufgeklärt werden. Zu den möglichen Nebenwirkungen gehören vor allem Übelkeit, Bauchkrämpfe, Durchfall, starkes Schwitzen und ein verlangsamter Herzschlag (Bradykardie).
Eine Rückbildung der Symptome durch einen Cholinesterasehemmer allein ist nur bei etwa zehn Prozent der Betroffenen zu erreichen. In den meisten Fällen ist eine Kombination mit einem das Immunsystem unterdrückendem Medikament (Immunsuppressivum) notwendig. In erster Linie werden Glucocorticoide (Kortison) wie Prednisolon verwendet. Auch hierbei sind Nebenwirkungen zu beachten, insbesondere bei der längerfristigen Anwendung. Die Dosierung sollte dementsprechend mit einem erfahrenen Spezialisten abgesprochen werden. Eine weitere Option stellt das Immunsuppressivum Azathioprin dar. Es kann sowohl allein als auch in Kombination mit Prednisolon angewendet werden.
Viele Betroffene profitieren außerdem von der operativen Entfernung der Thymusdrüse, unabhängig davon, ob sie krankhaft verändert ist oder nicht. Die Beratung sollte hierzu im Einzelfall durch einen Arzt erfolgen.
Generell sollten Betroffene auf eine gesunde Lebensweise und ausgewogene Ernährung mit ausreichend Vitaminen, Mineralien und Spurenelementen achten. Außerdem können begleitende Therapien und Hilfsmittel sinnvoll sein. Dazu gehören zum Beispiel Logopädie bei Sprachstörungen, eine Halskrause bei Kopfhalteschwäche und Gehhilfen (Rollator, Rollstuhl).
Neue Therapien bei Myasthenia gravis
Neue Ansätze in der Therapie der Myasthenia gravis zielen auf eine gezieltere Unterdrückung der Immunreaktion. Infrage kommt zum Beispiel ein Antikörper, der gegen bestimmte Abwehrzellen des Körpers (B-Zellen) gerichtet ist. Es handelt sich um Rituximab, das bereits bei anderen Erkrankungen (unter anderem Leukämien und Autoimmunerkrankungen) eingesetzt wird.
Außerdem kann Eculizumab zum Einsatz kommen. Dabei handelt es sich um einen Antikörper gegen einen anderen Bestandteil des Immunsystems, den Komplementfaktor C5.
Welche Medikamente sind tabu?
Es existieren einige Medikamente, die bei Myasthenia gravis gemieden oder nur mit äußerster Vorsicht eingenommen werden sollten. Jeder behandelnde Arzt ist unbedingt über die eigene Erkrankung zu informieren. Vor Einnahme neuer Medikamente sollte in jedem Fall Rücksprache mit einem Spezialisten gehalten werden.
Zu den "verbotenen" Medikamenten bei Myasthenia gravis zählen:
- einige Antibiotika der Gruppe der Aminoglykoside (Streptomycin, Neomycin, Gentamicin), Fluorchinolone (Levofloxacin, Ciprofloxacin), Glykopeptide (Vancomycin), Lincosamide (Clindamycin) und Makrolide (Erythromycin)
- Antidepressiva (Amitriptylin)
- Antikonvulsiva (Benzodiazepine, Carbamazepin, Gabapentin)
- Antimalariamittel (Chinin, Chloroquin)
- Antirheumatika (D-Penicillamin, Chloroquin)
- Botulinumtoxin (Botox)
- Diuretika (Schleifendiuretika, Thiaziddiuretika)
- Interferon-α
- Calciumantagonisten
- Lithium
- Muskelrelaxantien
- Magnesiumpräparate
Prognose bei Myasthenia gravis
Die Einnahme der Medikamente ist in den meisten Fällen lebenslang notwendig. Damit gehen gewisse Risiken und Nebenwirkungen einher. Allerdings kann durch die Medikation eine Remission (Rückbildung) der Symptome erreicht werden, sodass eine normale Lebenserwartung und eine gute Lebensqualität möglich sind.
Lebensgefährlich ist vor allem die myasthene Krise bei dramatischer Verschlechterung der Symptomatik mit Beeinträchtigung der Atmung. Dieser Notfall kann durch sachgemäße Behandlung jedoch zum Glück vermieden werden.